晁代印研究组发现植物种子铁含量关键基因,有望解决“隐性饥饿”问题
2021年9月4日,Science子刊Science Advances 发表了中国科学院分子植物科学卓越创新中心晁代印研究组题为 “NPF transporters in synaptic-like vesicles control delivery of iron and copper to seeds” 的研究论文。该研究首次鉴定到长久以来植物营养学家所关注的植物中铁运输关键基因NAET1和NAET2,发现这两个基因编码蛋白能够以类似动物神经递质释放的方式将铁运输关键小分子化合物nicotianamine (NA)分泌到细胞外,从而帮助植物体内铁、铜等离子的长距离运输,促进它们在籽粒中的积累。
铁营养缺乏是目前全球最严重的营养问题之一,它可以造成缺铁性贫血病、儿童发育迟缓以及记忆力衰退等疾病,所以这类微量元素缺乏的问题又被称为“隐性饥饿” 。据世界卫生组织调查显示,全球约20亿人面临着缺铁引起的健康问题,其中又以孕妇和儿童最为严重。这是因为大多数植物来源的主食含铁量极低,并且其中的抗营养因子还会进一步阻碍人体对铁的吸收效率。植物中铁元素的运输必须依赖于一系列小分子螯合物的结合,形成稳定、易溶的铁合物复合体,再通过一系列的转运蛋白将铁运输到需要的各个器官,而NA就是其中最为关键的一种。NA是植物中特有的一种非编码氨基酸,它可以与铁及其他二价阳离子形成稳定的螯合物从而促进这些离子的长距离运输。有趣的是,NA也是促进人类和动物铁吸收的最佳增强剂,同时还有助于预防老年痴呆和高血压,因此其在植物中的运输和积累不仅对于植物本身具有重要意义,对于人类健康同样具有重大价值。然而,NA在细胞质中合成之后如何被运送到细胞之外,如何转运到籽粒,并如何协助铁离子的长距离运输,一直是植物营养领域的未解之谜。
这项研究巧妙的运用无法合成及运输NA的酵母异源表达体系,筛选到拟南芥中硝酸根/寡肽运输蛋白家族(NPF)成员NPF5.8和NPF5.9能将酵母细胞质内异源合成的NA分泌到细胞外,因此将这两个蛋白名为NAET1(NA efflux transporter 1)和NAET2(NA efflux transporter 2)。利用CRISPR-Cas9技术敲除产生的单基因突变体与野生型Col-0相比在生长和离子组方面无明显差异,但其杂交产生的双突变体naet1naet2 地上部整体发黄,种子发育迟缓、难以萌发。此外,该双突变体幼叶、花及种子中NA含量急剧降低,而根部NA却显著升高,表明NA在植物体内的运输受阻。离子组检测发现,双突变体naet1naet2种子、花及幼叶中的铁、铜和钴均大幅降低,而老叶中则铜、钴含量降低,铁含量无差异。结合嫁接实验、木质部和韧皮部流检测结果表明两个NAET蛋白通过控制根部木质部流中NA的含量调控了木质部中铜和钴的转运,并通过控制地上部韧皮部NA的含量控制韧皮部铁和铜的长距离运输,而这一结果与前人研究发现的不同金属离子-NA复合体在不同pH环境下的动力学特性完美吻合。而进一步组织分布的研究发现这两个NAET编码基因主要在根、茎和叶片的维管束中高表达,表明NAET1和NAET2直接控制NA在木质部和韧皮部的分泌和装载。有趣的是,绿色荧光融合蛋白显示NAETs并不位于NPF家族蛋白常在的细胞表面质膜上,而是定位在细胞内一种特殊的囊泡上。免疫荧光实验证实这种囊泡正是NA富集的地方,而阻止这种囊泡的运动就能阻止NA的分泌。利用异源表达NAET蛋白的酵母微粒体进一步证实了NAET可以将NA运输到这种囊泡中。
这些结果表明细胞质内合成的NA通过NAET蛋白的运输储存到这种特殊的囊泡中,并进一步通过囊泡运输以胞吐的方式释放到细胞外,而金属离子在细胞外与NA结合后进入木质部或韧皮部进行长距离运输。这种物质外排的方式与动物的神经递质的释放方式极为相似。这种方式曾被认为是动物所特有的物质运输方式,而在植物中并不存在。因而,此项研究发现了影响植物种子铁、铜等离子运输和积累的关键基因,为解决人类铁营养缺乏,改善人类生命健康提供了全新视角和方案,同时也拓展了人们过去对于植物营养物质运输方式的认识,深化了人们对于植物和动物界限的理解。
中国科学院分子植物科学卓越创新中心晁代印研究员为该论文的通讯作者,博士生晁振飞为第一作者,雷明光研究员和华中农业大学严建兵教授参与了研究。该研究得到国家自然科学基金重点项目、中科院先导项目、四川省地区联合基金项目和英国皇家学会牛顿基金高级学者项目的资助。
论文链接:https://www.science.org/doi/10.1126/sciadv.abh2450
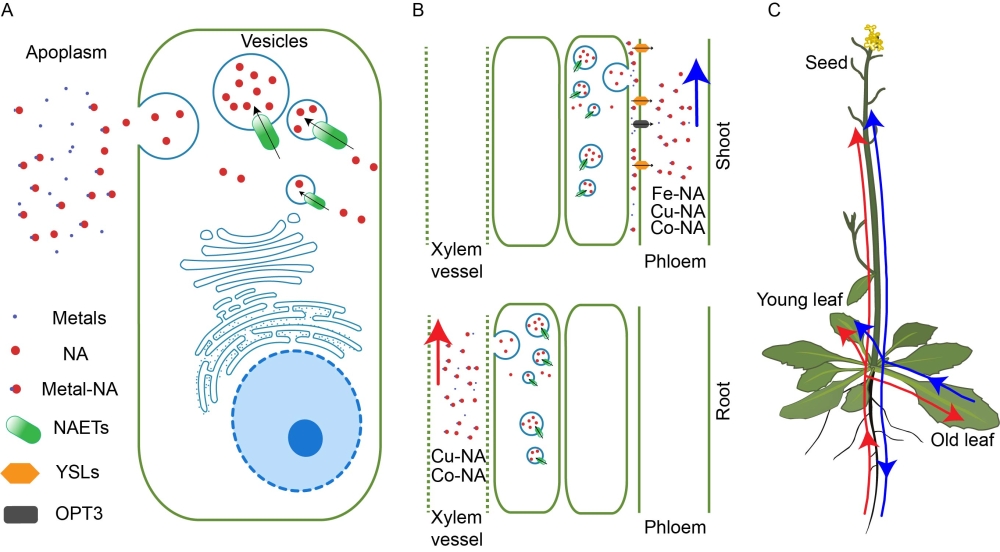
NAETs调控离子稳态模型