万里研究组揭示植物helper免疫受体细胞膜定位和抗病小体形成的机制
植物依赖细胞内免疫受体NLR识别病原菌分泌进入胞内的效应因子(effector),并触发ETI (Effector-Triggered Immunity) 免疫。NLR蛋白根据其N末端结构域可分为三类:TIR-NLR (TNL),CC-NLR (CNL) 和 CCR-NLR (RNL);根据NLR发挥功能的方式可分为两类:识别effector并起始ETI信号的sensor NLR,和作用于sensor NLR下游并进一步转导免疫和细胞死亡信号的helper NLR。TNL 和 CNL 一般作为sensor NLR发挥功能。RNL家族中的ADR1和NRG1,以及在茄科中特异存在的NRC(一类特殊的 CNL)是已知的helper NLR。目前的模型大致认为helper NLR激活后在细胞膜上多聚化形成抗病小体并作为钙离通道发挥功能,但helper NLR实现细胞膜定位的机制以及形成抗病小体的过程和组分还不清楚。
2023年7月31日,中国科学院分子植物科学卓越创新中心万里团队在PNAS在线发表题为“Plasma membrane association and resistosome formation of plant helper immune receptors”的研究论文。该成果首先揭示植物中的三类helper NLRs(包括NRG1, ADR1 和 NRC)在激活前后都是通过其N端结构域 (CC或CCR) 中保守的正电氨基酸残基 (K/R) 与细胞膜上带负电荷的磷脂互作而定位在细胞膜上。进一步的研究发现被effector激活的TNL可以诱导NRG1的多聚化,且多聚化的NRG1抗病小体中可能只含有NRG1分子。
该研究首先对不同物种中三类helper NLR的CCR和CC进行蛋白序列比对,发现这个结构域的第2和第4个α螺旋中存在保守的正电荷氨基酸残基位点(K/R),且该保守K/R残基旁侧且会高频富集正电氨基酸残基。在此基础上对该保守K/R位点及其临近的正电氨基酸进行突变分析。进一步利用protein lipid overlay assay、亚细胞定位分析 (荧光共聚焦和亚细胞组分分离提取) 和细胞死亡表型分析等技术,确定了鉴定到的保守(K/R)位点对三类helper NLR激活前后膜定位以及发挥细胞死亡功能的重要性。
NRG1在TNL下游介导细胞死亡信号通路,且NRG1需要脂肪酶类似蛋白EDS1和SAG101协同发挥功能。本研究表明effector 激活TNL后会诱导NRG1的多聚化并在细胞膜上形成puncta。研究利用各种高度特异性的NRG1突变体(多聚化增强或丧失,细胞膜定位缺失和钙离子通道活性丧失)进一步说明puncta的形成与NRG1的多聚化能力高度相关且effector激活的NRG1依赖膜定位和钙通道活性发挥功能。此外作者还发现细胞质定位的EDS1/SAG101是effector激活 NRG1导致细胞死亡的必要条件,但非变性胶的结果则显示在多聚化的NRG1抗病小体中并检测不到EDS1/SAG101的参与。暗示NRG1通过与EDS1/SAG101互作被激活后,可能有其他未知信号导致EDS1/SAG101与NRG1的解离和最终NRG1寡聚体的形成。
中国科学院分子植物科学卓越创新中心的博士后王再青和刘晓晓为论文的共同第一作者,中国科学院分子植物科学卓越创新中心万里研究员为通讯作者。美国北卡罗来纳大学教堂山分校生物系的Jeffery L. Dangl教授和Nak Hyun Kim博士,以及德国图宾根大学植物分子生物中心的Farid EI Kasmi博士参与了该研究工作。中国科学院分子植物科学卓越创新中心喻杰博士,技术服务平台的殷水宁老师和蔡文娟老师对该研究提供了宝贵的技术支持。该研究得到中科院先导B专项、植物分子遗传国家重点实验室、国家自然科学基金和国家博士后基金的资助。
论文链接:www.pnas.org/doi/10.1073/pnas.2222036120
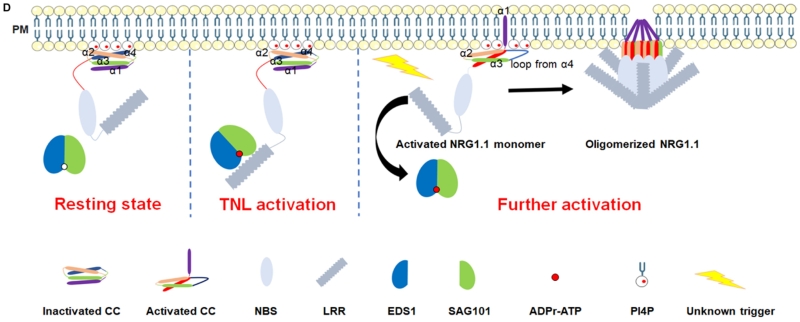
植物helper NLR细胞膜定位和抗病小体形成的机制